https://doi.org/10.22319/rmcp.v13i1.5741
Nota de investigación
Efecto de la nisina en la inhibición del crecimiento de Staphylococcus areus y en las propiedades sensoriales del queso costeño
Beatriz Alvarez Badel a*
Maria Alejandra Doria Espitia a
Vanesa Hodeg Peña a
Mónica María Simanca Sotelo a
Yenis Pastrana Puche a
Claudia Denise De Paula a
a Universidad de Córdoba. Departamento de Ingeniería de alimentos, Sede Berástegui, Vía Cereté – Ciénega de Oro, Córdoba, Colombia.
*Autor de correspondencia: bealvarez@correo.unicordoba.edu.co
Resumen:
Se evaluó el efecto de la adición de nisina en queso costeño obtenido en la ciudad de Montería – Córdoba, Colombia, sobre la inhibición del crecimiento de Staphylococcus aureus y sobre las características sensoriales del queso. Se obtuvieron muestras de queso costeño en 9 comercializadoras de la ciudad y se aisló S. aureus, se determinó la concentración mínima inhibitoria (CMI) con nisina; se elaboró queso costeño con la adición de nisina a 0, 500 y 625 UI/kg. Se realizó el recuento de S. aureus, a las 0 y 24 h de almacenamiento; se estableció un diseño completamente al azar con 57 unidades experimentales. Se realizó una prueba triangular con panel de 40 catadores para determinar diferencias sensoriales entre el queso costeño tradicional y con adición de nisina. Se determinó que el queso costeño presentó contaminación por S. aureus; dichas cepas fueron inhibidas con una CMI de nisina de 500 UI/ml. Los recuentos de S. aureus en queso costeño adicionado con nisina presentaron diferencias significativas (P≤0.05) con el testigo; se observó que después de 24 h la nisina redujo de 2.3 ciclos logarítmicos para concentración de 500 UI/kg y 1.9 ciclos logarítmicos para 625 UI/kg. El queso costeño adicionado con 500 UI de nisina/kg no presentó diferencias (P≥0.05) en las propiedades sensoriales con relación al testigo. Se concluye que la nisina a 500 UI/ml inhibe al S. aureus aislado del queso costeño comercializado en la ciudad de Montería- Córdoba.
Palabras clave: Bacteriocinas, Concentración mínima inhibitoria, S. aureus.
Recibido: 22/07/2020
Aceptado:12/05/2021
La inocuidad de los alimentos engloba acciones encaminadas a garantizar la máxima seguridad posible de los alimentos. Se puede definir inocuidad como la garantía de que el alimento no genere peligros biológicos, físicos o químicos al consumidor, la ausencia de sustancias peligrosas, la certeza de ausencia de efectos adversos o lo contario al riesgo(1). Dentro de los riesgos biológicos en los alimentos se encuentra la presencia de microorganismos patógenos; uno de ellos es Staphylococcus aureus, bacteria Gram positiva de la flora normal del hombre, con capacidad de desarrollarse en muchos alimentos (carnes rebanadas, leche y derivados, salsas, conservas, productos de panaderías, cremas de huevos, entre otros) y producir la intoxicación estafilocócica con una ingesta mínima de 100 ng de toxina(2).
El queso costeño es un alimento autóctono de la Costa Caribe colombiana; es un producto artesanal realizado a partir de leche no pasteurizada, con coagulación enzimática, prensado, no madurado, ni acidificado, de color blanco, que se somete a un salado en seco y se elabora bajo mínimas condiciones sanitarias; por ser un producto de la canasta básica de la región, se incrementa el riesgo de intoxicación alimentaria(3). La Norma Técnica Colombiana NTC 750, estipula los criterios microbiológicos para dicho producto, y establece que el recuento de S. aureus coagulasa positiva debe encontrarse en un rango de 100 a 1,000 UFC/g(4).
Se han encontrado valores no aceptables de Staphylococcus coagulasa positiva en el 41.4 % de las muestras de queso costeño expedido en Montería-Córdoba(5). Estudios con queso costeño expendido en Valledupar-Cesar demostraron la presencia de S. aureus en el 75 % de los quesos costeños blandos y 25 % de los quesos semiduros estudiados(6). Una de las alternativas utilizadas para inhibir a S. aureus es el uso de la nisina, un conservante alimentario permitido por FDA, por su categoría GRAS (Generally Recognized As Safe). La nisina es una sustancia polipeptídica producida por diferentes cepas de Lactococcus lactis y Streptococcus lactis. Actúa frente a las bacterias Gram positivas, es estable en pH ácido y ligeramente termosensible. Se conoce como E234 y es empleada en la industria alimentaria, principalmente en la elaboración de quesos(7). Los quesos son la matriz alimentaria donde se ha estudiado con más frecuencia, especialmente S. aureus es el tercer microorganismo más estudiado(8).
Para cuantificar la actividad in vitro de un antimicrobiano frente a un cultivo bacteriano se utilizan técnicas de dilución en caldo o agar, como la concentración mínima inhibitoria (CMI), en donde se preparan una serie de tubos o placas con caldo o agar, respectivamente, a los cuales se les agrega el antimicrobiano estudiado en distintas concentraciones, luego se inoculan cada uno de los tubos o las placas con una suspensión estandarizada del microorganismo en estudio. La lectura e interpretación de la CMI corresponde a la mínima concentración de bactericida en donde no se observa desarrollo (turbidez) y se expresa en μg/ml(9).
El objetivo de esta investigación fue evaluar el efecto de la nisina a través de la técnica de concentración mínima inhibitoria sobre S. aureus aislado del queso costeño comercializado en queseras oficialmente registradas en el municipio de Montería – Córdoba, Colombia.
Aislamiento e identificación de S. aureus. Se visitaron las empresas expendedoras de queso costeño en la ciudad para obtener muestras de 250 g de queso y se trasladaron al Laboratorio de Microbiología de Alimentos de la Universidad de Córdoba, Colombia. Se obtuvieron diluciones seriadas y se sembraron por duplicado en superficie en placas con agar sal y manitol por 24 a 48 h a 37 ºC(10). Se realizaron pruebas confirmativas a las colonias características de S. aureus, por tinción de Gram, prueba de catalasa y coagulasa(11). Se aplicó técnica de PCR en tres de las cepas obtenidas(12). Se almacenaron a temperatura de 2 a 4 °C. Se activaron con caldo nutritivo y siembra en agar Baird Parker (BPA).
Determinación de CMI de la nisina sobre las cepas de S. aureus aislado de queso costeño. Se realizó una escala de McFarland como patrón de turbidez para estandarizar la densidad en preparaciones de microorganismos. La escala de 0.5 fue preparada con ácido sulfúrico (0.18 M) y una solución acuosa de cloruro de bario (0,048 M) equivalente a 1.5 x 108 UFC/m y una densidad óptica de 0.08 a 0.12 a 625 nm(13). En tubos con 5 ml de caldo Mueller Hilton (MH) se adicionaron tres colonias de S. aureus, se incubaron a 37 °C durante 1 h. Se realizaron mediciones de absorbancia y turbidez. Los tubos que presentaron la medida de absorbancia y turbidez dentro del rango establecido se consideraron estandarizados en la escala 0,5 McFarland con aproximadamente 1.5 x 108 células/ml(14).
Posteriormente se preparó una solución madre de nisina (NISIN(z) Qiqihaer Heilongjiang Province China del Laboratorio Amtech Biotech, HS Code 2941909090), diluyendo 1.0 g de nisina en 100 ml de HCl al 0,02 N, esta solución contenía 1.0 x 104 UI/ml con pH cercano a 2.0, y se ajustó el pH a 3.21 con NaOH al 0.5 N. Esta solución se diluyó con caldo Mueller Hinton (MH) para conseguir concentraciones de 100, 200, 500, 1,000, 1,500, 2,000 y 2,500 UI/ml(15). Como testigo se utilizó caldo MH. A cada uno de los tubos se le agregaron 10 µl del inóculo preparado con S. aureus, y se incubaron a 37 °C por 24 h con agitación a 182 rpm.
Para realizar la curva de letalidad, se realizó el procedimiento con las concentraciones de ½ CMI, CMI, 2xCMI y 4xCMI; se sembró por triplicado el contenido de los tubos en placas de agar Baird Parker a diferentes tiempos de incubación (0, 2, 4, 8, 20 y 24 h) y se realizó el recuento de número de colonias; se elaboró una gráfica recuento bacteriano (UFC/ml) vs el tiempo de exposición (horas)(11). La gráfica exhibe una cinética exponencial de primer orden, cuya fórmula es 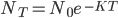 , mediante la aplicación de logaritmos se transforma en
, mediante la aplicación de logaritmos se transforma en 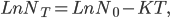 se obtiene la tasa de letalidad (K). Despejando la ecuación anterior se puede calcular el tiempo que tarda la población del microorganismo en reducirse a la mitad, conocido como tasa de letalidad: T1/2 = ln2/K(16).
se obtiene la tasa de letalidad (K). Despejando la ecuación anterior se puede calcular el tiempo que tarda la población del microorganismo en reducirse a la mitad, conocido como tasa de letalidad: T1/2 = ln2/K(16).
Evaluación de diferentes concentraciones de nisina en la elaboración de queso costeño. Para la elaboración de queso costeño se realizó el siguiente proceso(17). A la leche filtrada se le analizó el pH (potenciometría), acidez(18) y recuento de S. aureus(11). Se calentó la leche a 34 ± 1 ºC y se adicionó CaCL2 (20 g/100 L de leche) y se adicionó cuajo liquido Milkset (1.0 ml /10.0 L de leche). La cuajada se cortó en cuadros de 1 a 2 cm y se dejó en reposo por 5 min. Se separó el suero por gravedad y se adicionó sal directamente a 2.5 %. La cuajada salada se separó en tres lotes de 500 g y se adicionó nisina distribuida de forma homogénea (625, 500 y 0.0 UI/kg). El material se llevó al molde y se prensó. De cada uno de los lotes se tomaron muestras, las que se almacenaron a 4 ± 2 °C y se realizó el recuento de S. aureus por triplicado a 0 y 24 h de acuerdo al procedimiento señalado por Silva et al(11).
Se utilizó un diseño completamente al azar con 57 unidades experimentales. Los datos se analizaron a través de software estadístico R Project versión 3.1.1. Se realizó un análisis de varianza y una vez comprobadas diferencias estadísticas entre los tratamientos se realizó una prueba de rangos múltiples de Duncan (P<0.5), con el fin de determinar si existían diferencias significativas entre los recuentos de S. aureus de las muestras de queso sin nisina y los elaborados con las concentraciones ensayadas de nisina.
Aplicación de prueba triangular a los quesos costeño tradicional y elaborado con nisina. Se utilizaron 40 catadores no entrenados, con edades comprendidas entre los 19 y 45 años; se evaluó si existían diferencias sensoriales significativas entre los quesos costeño y costeño adicionado con nisina a 500 UI/kg; concentración máxima permisible de acuerdo con la Norma Estándar para quesos del Codex Alimentarius(19). Para la evaluación sensorial de los quesos se presentó un grupo de tres muestras, donde dos eran iguales entre sí y se le pedía al catador seleccionar la muestra diferente. Se tabuló el número de aciertos obtenidos por los catadores y se compararon con el cuadro: número mínimo de juzgamientos correctos para establecer significancia en distintos niveles de probabilidad para la prueba triangular (una cola, P = 1/3)(20).
Aislamiento, selección e identificación de S. aureus a partir de queso costeño. En todas las muestras de queso costeño estudiadas se aisló S. aureus. En total se encontraron 18 cepas con colonias características de S. aureus (redondas, rodeadas de una zona amarilla brillante). Las cepas asiladas caracterizadas de acuerdo con su morfología celular, colonial, y bioquímica correspondieron a S. aureus; en los resultados obtenidos por PCR se identificaron que tres cepas estudiadas contenían los genes que codifican para la enterotoxina de S. aureus.
Determinación de la CMI sobre cepas de S. aureus aislado de queso costeño. Se determinó que la concentración de 500 UI/ml inhibió al S. aureus, ya que luego de 24 h de incubación no se observó turbidez, contrario a lo ocurrido en los tubos con concentraciones de 100 y 200 UI/ml. Se amplió el rango de concentraciones de estudio entre 500 y 1125 UI/ml, y se observó inhibición a 625 UI/ml.
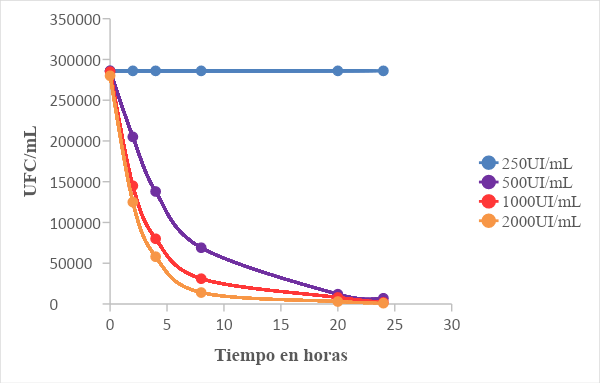
Curva de letalidad. En la Figura 1 se presentan las curvas de letalidad para S. aureus expuesto a cuatro concentraciones de nisina; se observa que en las concentraciones de nisina iguales o superiores a la CMI los recuentos disminuyen logarítmicamente, evidenciando la acción de la nisina sobre el microorganismo, pero con la concentración de 250 UI/ml, los recuentos en el tiempo se mantienen constantes, lo que sugiere que la nisina a esa concentración no inhibe al S. aureus. A través de la curva se logra visualizar la dinámica sobre la relación entre la concentración de nisina y su actividad bactericida, por lo que es necesario graficar el logaritmo del número de células sobrevivientes (UFC/ml) versus el tiempo.
Figura 1: Curva de letalidad de Staphylococcus aureus en relación con la concentración de nisina en agar Baird Parker
La Figura 2 permite apreciar el tiempo en que la concentración es bactericida, es decir el tiempo en el que el descenso de UFC es de tres ciclos logarítmicos con respecto al tiempo inicial(21). El tiempo en que la concentración alcanzó su mayor acción bactericida; para 500 UI/ml fue de 20 h. Por medio de los resultados se puede afirmar que a las 24 h de incubación la nisina a una concentración de 500 UI/ml logró una disminución significativa de la carga bacteriana de 3.7log (UFC/ml).
Figura 2: Número de células sobrevivientes (Log UFC/g) vs el tiempo en horas
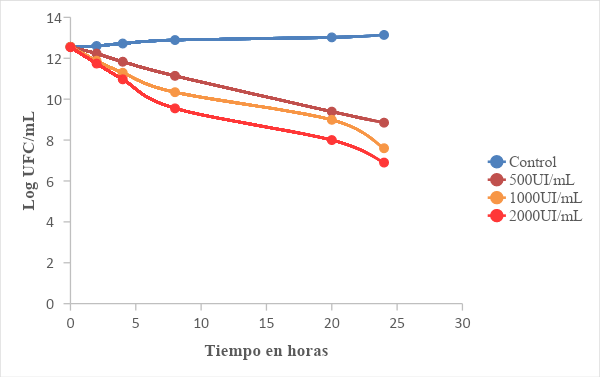
También se observa que los recuentos disminuyeron proporcionalmente con el tiempo de incubación. En el cuadro 1 se presentan las pendientes de cada ecuación obtenida, la cual corresponde a la tasa de letalidad (UFC/hora). Se infiere que a mayor concentración mayor es la velocidad de muerte del microrganismo.
Cuadro 1: Tasa de letalidad y tiempo de reducción de la población de Staphylococcus aureus para las concentraciones de nisina evaluadas
Nisina (UI/ml) | K (UFC/horas) | T1/2 (horas) |
500 | 0.154 | 4.50095572 |
1000 | 0.184 | 3.76710424 |
2000 | 0.205 | 3.38120576 |
Evaluación de diferentes concentraciones de nisina en la elaboración de queso costeño. En la leche utilizada en la elaboración de los quesos se midieron valores promedios de pH de 6.8 y acidez de 0.16 % (ácido láctico), los cuales estaban de acuerdo a los parámetros establecidos en la normatividad colombiana; en cambio, los recuentos de S. aureus superaron a 10,00 UFC/ml(22).
En el Cuadro 2 se muestran los promedios de los recuentos en UFC/g para los tratamientos evaluados; en los lotes con concentración de 625 y 500 UI/kg de nisina se presentó un recuento menor de S. aureus respecto a los resultados del tercer lote, tratamiento sin nisina. Los recuentos del tercer lote se encontraron por encima del límite máximo permisible 103 UFC/g de S. aureus a las 0 y 24 h; representando un riesgo de intoxicación alimentaria. El análisis de varianza estableció que existían diferencias significativas (P<0.05), en cada uno de los tratamientos estudiados para los dos tiempos de almacenamiento evaluados, es decir que las concentraciones de nisina aplicadas en el queso costeño afectaron significativamente los recuentos de S. aureus.
Cuadro 2: Comparación de medias para el promedio del recuento de Staphylococcus aureus en los lotes de queso costeño a las cero y 24 horas de almacenamiento
| Medias de recuento (UFC/g) 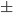 S D S D |
|
Tratamiento nisina (UI/kg) | Cero horas |
| 24 horas |
| Reducción (B/A,%) |
625 | 69.9 ± 49.1 | a | 11.1 ±9.2 | a | 15.9 |
500 | 658 ±254 | ab | 64.4 ±53.6 | a | 9.8 |
Sin nisina | 1669 ±609 | c | 2403±738 | b |
|
abc Las letras diferentes indican que las medias difieren entre sí (P<0.05).
En el Cuadro 2 se observa que todos los tratamientos aplicados a las cero horas difieren entre sí, evidenciando que la adición de nisina a una concentración de 625 UI/kg logró la mayor disminución de la carga de S. aureus en el queso costeño. En los recuentos a las 24 h se encontraron diferencias (P<0.05) entre los recuentos de las muestras de queso sin nisina y de queso con nisina a 625 y a 500 UI//kg, lo que sugiere que las dos concentraciones de nisina tienen efecto similar en la inhibición de S. aureus.
En la Figura 3 se presenta los valores promedios de las poblaciones de S. aureus en cada una de las muestras de queso costeño analizadas durante el almacenamiento y la diferencia en ciclos logarítmicos. En las muestras de queso costeño sin nisina el recuento del microorganismo aumentó a medida que transcurrió el tiempo de almacenamiento. La diferencia entre los recuentos de S. aureus del control con el tratamiento de 500 UI/kg son 3.62 ciclos logarítmicos.
Figura 3: Promedio del recuento de Staphylococcus aureus para las concentraciones de nisina y testigo en los tiempos de almacenamiento
Resultado de la prueba sensorial. Los resultados obtenidos por el grupo de catadores en la prueba triangular indican que no existieron diferencias (P<0.05) entre el queso costeño elaborado de forma tradicional y al que se le agregó 500 UI de nisina, lo que sugiere que la nisina no produce ninguna alteración de las propiedades sensoriales apreciables en el producto.
La presencia S. aureus en las muestras de quesos costeños estudiados, reveló que la población cordobesa consumidora de este producto se encuentra expuesta al riesgo de intoxicación alimentaria; la presencia de este microorganismo en el queso costeño se puede relacionar con la falta de pasteurización y malas prácticas higiénicas en la manipulación, distribución y venta de dicho producto. En Colombia se reportaron 881 brotes de enfermedades transmitidas por alimentos en el año 2018, en las cuales, el queso estuvo presente en el 19.4 % de los brotes. En los casos donde se identificó el agente etiológico, 12 % resultó ser S. aureus(23). Estudios de queso costeño expedido en el departamento de Córdoba han catalogado al producto como no apto para el consumo humano por la significativa carga microbiológica observada, y lo asociaron a las deficiencias higiénicas en la manipulación del producto y a los defectos de las instalaciones existentes en los locales donde se comercializan(5).
En la mayoría de los locales visitados en el estudio se observaron condiciones insuficientes en la distribución, almacenamiento y venta del producto; sólo en pocos establecimientos se conservaba el producto en refrigeración. Es muy probable que esas condiciones afectaban directamente la calidad microbiológica del queso costeño. Por ello se ha sugerido revisar la aplicación de buenas prácticas de manufactura en su procesamiento, ya que la contaminación por S. aureus en quesos artesanales puede originarse de la piel, boca o fosas nasales de los manipuladores del alimento, de la leche cruda, de las condiciones de proceso y ambientales(24). Estudios previos han evaluado la calidad higiénica de quesos artesanales realizados con leche cruda en diversas localidades, y todos han asociado la presencia de S. aureus, con una baja calidad higiénica(25-28). Es claro que en los quesos artesanales donde no se utilizaban cultivos iniciadores, S. aureus no tenía flora competidora, como las bacterias ácido lácticas, y presentaba un riesgo significativo para la producción de toxinas si los recuentos iniciales son suficientemente altos(29).
En el presente estudio la concentración de nisina requerida para inhibir a S. aureus, fue de 500 UI/ml; diversos estudios con quesos artesanales concuerdan con estos resultados. En Brazil evaluaron el efecto de la nisina en queso artesanal de Araxá (Minas Gerais) contaminado con S. aureus, reportando mayor inhibición con concentraciones de nisina de 400 y 500 UI/ml en 10 días de almacenamiento(30); también reportaron que las concentraciones de 100 UI/ml redujeron un ciclo logarítmico en el recuento del microorganismo en 60 días de almacenamiento, sin cambiar atributos como el color y la textura(31). Han relacionado reducciones de 2 ciclos logarítmicos en el recuento de S.aureus en cuajada y suero de queso fresco de Minas Gerais elaborado con leche que contenía 500 UI/ml de nisina. En el queso redujo 1.5 ciclos logarítmicos en 30 días de almacenamiento refrigerado, y en la leche alargó 8 h la fase de latencia en el crecimiento del S. aureus(32). Estudios con queso costeño elaborado con leche pasterizada inocularon cepas de S. aureus ATCC 29213 encontrando CMI de nisina de 500 UI/ml(33).
El efecto antibacteriano de la nisina, se ha explicado como una despolarización de la membrana citoplasmática, la que consiste en una acción dual sobre la membrana de los microorganismos, primero le forma poros y también actúa como un detergente que la desestabiliza(34). Este efecto se realiza en tres pasos, inicia con la interacción de su carga positiva con la carga negativa de la pared celular, seguido se une a una molécula transportadora de peptidoglucano del citoplasma a la pared celular (llamada lípido II), impidiendo su síntesis y, por último, las moléculas de nisina se unen al lípido II para fijarse y unirse a la membrana celular y formar poros, ocasionando la muerte celular(7).
La curva de letalidad microbiana sigue un comportamiento exponencial, con una cinética de primer orden porque existe linealidad entre el logaritmo de los supervivientes en relación con el tiempo de tratamiento. La pendiente de la curva simboliza la velocidad a la que mueren las células y es medida en UFC/tiempo. Es posible determinar el modelo matemático que mejor estime la pendiente, y determinar las UFC en cada tiempo y concentración; este modelo representa de manera óptima los datos obtenidos y permite comparar las diferentes cinéticas que presentan los antimicrobianos y antibióticos(35). Ya se han descrito parámetros cinéticos y modelos matemáticos para la inactivación de poblaciones microbianas en procesos térmicos, de presión y electromagnéticos(36). También se han descrito estos modelos de crecimiento, supervivencia o inactivación para diversos microorganismos expuestos a antimicrobianos naturales en diversas matrices alimentarias, y se ha generado información pertinente a través de ellos, como la duración de la fase de retraso, el tiempo de generación, densidad de población máxima y tasa de crecimiento exponencial(37). Específicamente se han enunciado que el modelo primario describe la inhibición de S. aureus en diversos tipos de carne(38).
Aunque existen antecedentes de investigaciones en queso costeño pasteurizado adicionado con nisina para inhibir a S. aureus, en este estudio se prefirió utilizar leche cruda para elaborar el queso costeño; se ha relacionado a la pasteurización con la destrucción de las enzimas, disminución del contenido de minerales y eliminación de microorganismos propios del área geográfica que proporcionan diferenciación del color y textura propios del queso, inclusive poseen potencial probiótico(39). En la leche se observó recuento inicial por encima de la norma colombiana, la presencia de S. aureus en productos lácteos indica contaminación por manipulación o enfermedad en el bovino por mastitis(40).
En la evaluación de las diversas concentraciones de nisina adicionadas en queso costeño, se observaron recuentos menores en la población de S. aureus, en los dos tiempos estudiados, a medida que la concentración de nisina aumentaba corroborando la relación inversa entre la concentración de nisina y el tiempo de reducción la población del microorganismo. Se registraron diferencias significativas en los recuentos de S. aureus en el tiempo cero demostrando el poder antimicrobiano de la nisina desde el momento de la adición. Estudios de viabilidad de S. aureus expuesto a la nisina durante 1 a 24 h evidenciaron que ocurre una reducción significativa de la población (P<0.01) dentro de la primera hora de exposición a la nisina(41).
El estudio en queso artesanal de Araxá (Minas Gerais-Brasil) evidencia este mismo comportamiento de S. aureus en leche adicionada con nisina, el cual tuvo mayor inhibición a las 8 h y a la vez, fue dependiente de la cantidad de nisina agregada en las diversas matrices(31). El queso costeño como matriz alimentaria con un contenido considerable de sal favoreció el efecto antimicrobiano de la nisina, por lo contrario, la presencia de lípidos lo interfirió, probablemente por su comportamiento anfipático(42). La mayor acción bactericida al principio pudiera estar relacionado con los siguientes factores: la rápida difusión de la nisina al aplicarse directamente al alimento(43), la resistencia microbiana adquirida o adaptativa que desarrolla el microorganismo en el tiempo en que se exponen al antimicrobiano(44), y la degradación que puede sufrir la nisina en el tiempo por las enzimas propias del alimento(45). Las muestras de queso costeño adicionado con nisina a 625 UI//kg y a 500 UI/kg, presentan una reducción significativa de 2.3 y 1.9 unidades logarítmicas respectivamente en 24 h. Aunque las dos concentraciones estudiadas inhiben a S. aureus, se debe utilizar en la industria 500 UI/kg de producto que es la concentración permitida por el Codex Alimentarius(18).
La evaluación sensorial del producto es de suma importancia porque evidencia que no se perciben cambios organolépticos (P>0.05) en el queso costeño adicionado con nisina 500 UI/kg respecto al queso tradicional; resultados similares fueron encontrados por Araujo et al(46) al adicionar 5 mg/kg de nisina en queso costeño. La nisina al ser una sustancia GRAS puede utilizarse en el producto de consumo humano de forma segura para la salud, con la tranquilidad de un menor recuento microbiano de S. aureus y la aceptación sensorial del producto por parte del consumidor.
Este estudio se evidencia una alta prevalencia de S. aureus en las muestras de queso costeño comercializadas en Montería – Córdoba, Colombia. Las cepas de S. aureus aisladas de queso costeño fueron inhibidas por el antimicrobiano nisina a una concentración de 500 UI/ml, el cual alcanzó su mayor acción bactericida a las 20 h de incubación, logrando una disminución de 3.7 Log (UFC/ml). La velocidad en que el microorganismo murió fue de 0.154 UFC/h con un tiempo de reducción de la población de 4.5 h. Las propiedades sensoriales del queso costeño elaborado con una concentración de nisina de 500 UI/kg de producto no presentaron diferencias significativas (P>0.05) con respecto al queso costeño elaborado de forma tradicional.
Literatura citada:
- Hassauer C, Roosen J. Toward a conceptual framework for food safety criteria: Analyzing evidence practices using the case of plant protection products. Saf Sci 2020;127:104683.
- Andrade FP, Medeiros BT, Barbosa TW, Silva ME. Fatores que propiciam o desenvolvimento de Staphylococcus aureus em alimentos e riscos atrelados a contaminação: uma breve revisão. Rev Ciênc Méd Biol 2019;18:8993.
- Arteaga MR, Hernández HL, Peñate CD. Elaboración de un queso procesado tipo untable obtenido a partir de queso costeño. Inf Tecnol 2020;31:187-194.
- ICONTEC. Instituto Colombiano de Normas Técnicas. NTC 750. Norma Técnica Colombiana sobre productos lácteos: Queso, 1-15, Colombia. 2009.
- Ruíz RA, Menco NY, Chams LM. Valoración microbiológica de queso costeño artesanal y evaluación higiénico-locativa de expendios en Córdoba, Colombia. Rev Salud Pública 2017;19:311-317.
- Acosta IP, José GG. Staphylococcus aureus procedentes de quesos costeños de Valledupar; susceptibilidad a antibióticos y perfil plasmídico. Rev Méd Risaralda 2019;25:14-14.
- Sánchez MA, Salgado MT, San-Miguel Á, Pachón Jesús, Rodríguez E, Pastor MR, Cabrero P. Nisina (N 234), aditivo utilizado como conservante en alimentos. Gac Med Bilbao 2019;116:166-173.
- Cano D, Gómez MA, Oviedo V, Rios LA. Nisina como conservante de alimentos: revisión sistemática de la literatura. Hechos Microbiol 2015;6:52-64.
- Yolanda H, Krajaejun T. Review of methods and antimicrobial agents for susceptibility testing against Pythium insidiosum. Heliyom 2020;6e03737.
- Abdel-Hameid AA, Saad NM, Valero A, Mahmoud S. Incidence of enterotoxigenic Staphylococcus aureus in milk and Egyptian artisanal dairy products. Food Control 2019;104:20–27.
- Silva N, Taniwaki MH, Junqueira VCA, Silveira NFA, Okazaki MM, Gomes RAR. Microbiological examination methods of food and water: a laboratory manual. 2nd ed. London, UK: Taylor & Francis Group; 2019.
- Løvseth A, Loncarevic S, Berdal KG. Modified multiplex PCR method for detection of pyrogenic exotoxin genes in staphylococcal isolates. J Clin Microbiol 2004;42:3869–3872.
- Shehu HA, Mukhtar AG, Adetoyinbo II, Ojo AO, Mus’ab UA. Phytochemical screening and antibacterial activities of cassia fistula leaf extracts on some selected pathogens. Int J Pharmacon Phytochem Res 2020;9:1779-1783.
- ASM. American Society for Microbiology. Kirby-bauer disk diffusion susceptibility test protocol. 2016.
- Marvdashti LM, Yavarmanesh M, Koocheki A. Controlled release of nisin from polyvinyl alcohol - Alyssum homolocarpum seed gum composite films: Nisin kinetics, Food Biosci 2019;28:133-139.
- Zhao X, Chen L, Zhao L, He Y, Yang H. Antimicrobial kinetics of nisin and grape seed extract against inoculated Listeria monocytogenes on cooked shrimps: Survival and residual effects. Food Control 2020;115:1-13.
- Pardo ME, Almanza F. Guía de procesos para la elaboración de productos lácteos. 1era ed. Bogotá, Colombia: Convenio Andrés Bello (CAB). 2005.
- ICONTEC. Instituto Colombiano de Normas Técnicas. NTC 4978. Leche y productos lácteos. Determinación de la acidez titulable (Método de referencia). 2001.
- FAO - OMS. Organización de las Naciones Unidas para la Alimentación y la Agricultura - Organización Mundial de la Salud. Codex Alimentarius. Leche y productos lácteos. Segunda ed. Roma. 2011.
- Lawless HT, Heymann H. Sensory evaluation of food. Principles and practices. 2nd ed. New York, USA: Springer; 2010.
- Ramírez L, Marin D. Metodologías para evaluar “in vitro” la actividad antibacteriana de compuestos de origen vegetal. Scientia et Technica 2009;15:263-268.
- MINSALUD. Ministerio de Salud y Protección Social. Decreto 616 del 2006. Reglamento Técnico sobre los requisitos que debe cumplir la leche para el consumo humano que se obtenga, procese, envase, transporte, comercialice, expenda, importe o exporte en el país. Bogotá, 2006.
- INS. Instituto Nacional de Salud. Boletín Epidemiológico Semana 52. ETAS. 2018.
- Martínez A, Ribot A, Riverón Y, Remón-Díaz D, Alelí Y, Jacsens L, Uyttendaele M. Staphylococcus aureus in the production chain of artisan fresh cheese. Rev Salud Anim 2019;41:2224-4700.
- Mehramuz B, Taghizadeh S, Kafil HS, Zonouzaq GY, Khiabani MS, Sheikhsaran E, Mokarram RR, Dehghani L. High rate of contamination with Staphylococcus aureus in traditional Koozeh cheeses. A molecular typing approach. Ann Ig 2020;32:178-185.
- Ferreira G, De Santa Helena AA, Madeira JT, Andrade JS, Mangiavacchi BM, Blanco PR, Neres A. Occurrence of Escherichia coli and Staphylococcus aureus in artisanal minas fresh cheeses produced in the rural area of the Baixada Fluminense region, Province of Rio de Janeiro, Brazil. WJPPS 2020;9:492-503.
- Ganz K, Yamamoto E, Hardie K, Hum C, Hussein H, Locas A, Steele M. Microbial safety of cheese in Canada. J Food Microbiol 2020;321:1-7.
- Silva TJ da, Silva AC da, Matos LG de, Silva M da, Camargo CH, Cobo R, Mores VL, Cirone NC. Enterotoxigenic potential and molecular typing of Staphylococcus sp. isolated from organic and conventional fresh minas cheese in the state of São Paulo, Brazil. Int Dairy J 2020;102:1-8.
- Donnelly C. Review of controls for pathogen risks in Scottish artisan cheeses made from unpasteurised milk. Food Standards Scotland. Inbhe Bidh Alba. Report v 4.7. 2018.
- Sobral D. Efeito da nisina na contagem de Staphylococcus aureus e nas características do Queijo Minas Artesanal da Região de Araxá. [Tesis doctoral]. Viçosa, Minas Gerais, Brazil: Universidad Federal de Viçosa; 2012.
- Sobral D, Soares M, Martins VA, Bueno RG, Jacinto JC, Fernandes A, Machado GM. Nisin reduces the Staphylococcus aureus count without changing the characteristics of Artisanal Minas Cheese from Araxá. Rev Inst Laticínios Cândido Tostes, 2019;74:185-196.
- Felicio BA, Pinto MS, Oliveira FS, Lempk MW, Pires ACS, Lelis CA. Effects of nisin on Staphylococcus aureus count and physicochemical properties of Minas frescal cheese. J Dairy Sci 2015;98:4364–4369.
- Campo MC. Determinación del efecto de una bacteriocina adicionada en queso costeño sobre Staphylococcus aureus [tesis Bacteriología] Montería, Córdoba, Colombia: Universidad de Córdoba; 2010.
- López MC. Aplicación de bacteriocinas para la bioprotección de alimentos [tesis doctoral] Andalucía, España: Universidad de Jaén. 2017.
- Rodríguez MR. Variabilidad de la inactivación microbiana y de la fase de latencia de los microorganismos supervivientes a un proceso de acidificación [tesis doctoral] Madrid, España: Universidad Complutense de Madrid. 2016.
- FDA. Food and Drug Administration. Kinetics of microbial inactivation for alternative food processing technologies. Overarching principles: kinetics and pathogens of concern for all technologies. J Food Sci 2000;65:1-118.
- Jaiswal AK, Jaiswal S. Modelling the effects of natural antimicrobials as food preservatives. In: Taylor M. Handbook of natural antimicrobials for food safety and quality. 1rst ed. Cambridge, UK: Woodhead Publishing Limited;2014:259-284.
- Ha J, Lee J, Lee S, Kim S, Choi Y, Oh H, Kim Y, Lee Y, Seo Y, Yoon Y. Mathematical models to describe the kinetic behavior of Staphylococcus aureus in Jerky. Food Sci Anim Resour 2019;39:371-378.
- Serpa JG, Pérez TI, Hernández EJ. Effect of pasteurization and starter cultures on physicochemical and microbiological properties of costeño cheese. Rev Fac Nac Agron 2016;69:8007-8014.
- INS. Instituto Nacional de Salud. Identificación de riesgos biológicos asociados al consumo de leche cruda bovina en Colombia. 2011.
- Jensen C, Li H, Vestergaard M, Dalsgaard A, Frees D, Leisner J. Nisin damages the septal membrane and triggers DNA condensation in Methicillin-Resistant Staphylococcus aureus. Front Microbiol 2020;11:1007.
- Heredia-Castro PY, Hérnández-Mendoza A, González-Córdova AF, Vallejo-Cordoba B. Bacteriocinas de bacterias ácido lácticas: mecanismos de acción y actividad antimicrobiana contra patógenos en quesos. Interciencia 2017;42:340-346.
- Coronado EP, Espitia R. Estudio del efecto de una película antimicrobiana en la vida útil del queso costeño [tesis Ingeniería de alimentos]. Berástegui, Colombia: Universidad de Córdoba; 2015.
- Serra MÁ. La resistencia microbiana en el contexto actual y la importancia del conocimiento y aplicación en la política antimicrobiana. Rev Habanera Cienc Médi 2017;16:402-419.
- FAO. Food and Agriculture Organization of the United Nations. Disposiciones sobre la ciclotetraglucosa (sin1504 i), El jarabe de ciclotetraglucosa (sin 1504 ii) y la nisina (sin 234). Programa conjunto FAO/OMS sobre normas alimentarias Comité del Codex sobre aditivos alimentarios. 47.ª reunión. Xi'an, China, 23 – 27 de marzo de 2015.
- Araujo D, Ávila L, Jiménez Y. Nisina: una bioalternativa para la reducción de las intoxicaciones alimentarias en el caribe colombiano. Lasirc 2020;1:59-64.
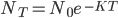 , mediante la aplicación de logaritmos se transforma en
, mediante la aplicación de logaritmos se transforma en 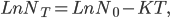 se obtiene la tasa de letalidad (K). Despejando la ecuación anterior se puede calcular el tiempo que tarda la población del microorganismo en reducirse a la mitad, conocido como tasa de letalidad: T1/2 = ln2/K(16).
se obtiene la tasa de letalidad (K). Despejando la ecuación anterior se puede calcular el tiempo que tarda la población del microorganismo en reducirse a la mitad, conocido como tasa de letalidad: T1/2 = ln2/K(16).